MODELO ATÓMICO DE RUTHERFORD.
El modelo de Rutherford fue el primer modelo atómico que consideró al
átomo formado por dos partes: la "corteza" (luego denominada
periferia), constituida por todos sus electrones, girando a gran
velocidad alrededor de un "núcleo" muy pequeño; que concentra toda la
carga eléctrica positiva y casi toda la masa del átomo.
Rutherford llegó a la conclusión de que la masa del átomo se
concentraba en una región pequeña de cargas positivas que impedían el
paso de las partículas alfa. Sugirió un nuevo
La importancia del modelo de Rutherford residió en proponer por
primera vez la existencia de un núcleo en el átomo (término que,
paradójicamente, no aparece en sus escritos). Lo que Rutherford
consideró esencial, para explicar los resultados experimentales, fue
"una concentración de carga" en el centro del átomo, ya que sin ella, no
podía explicarse que algunas partículas fueran rebotadas en dirección
casi opuesta a la incidente. Este fue un paso crucial en la comprensión
de la materia, ya que implicaba la existencia de un núcleo atómico donde se concentraba toda la carga positiva y más del 99,9% de la masa. Las estimaciones del núcleo revelaban que el átomo en su mayor parte estaba vacío.
Rutherford propuso que los electrones
orbitarían en ese espacio vacío alrededor de un minúsculo núcleo
atómico, situado en el centro del átomo. Además se abrían varios
problemas nuevos que llevarían al descubrimiento de nuevos hechos y
teorías al tratar de explicarlos:
- Por un lado se planteó el problema de cómo un conjunto de cargas positivas podían mantenerse unidas en un volumen tan pequeño, hecho que llevó posteriormente a la postulación y descubrimiento de la fuerza nuclear fuerte, que es una de las cuatro interacciones fundamentales.
- Por otro lado existía otra dificultad proveniente de la electrodinámica
clásica que predice que una partícula cargada y acelerada, como sería
el caso de los electrones orbitando alrededor del núcleo, produciría radiación electromagnética, perdiendo energía y finalmente cayendo sobre el núcleo. Las leyes de Newton, junto con las ecuaciones de Maxwell del electromagnetismo aplicadas al átomo de Rutherford llevan a que en un tiempo del orden de
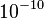 s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.2 Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.
s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.2 Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.
Según Rutherford, las órbitas de los electrones no están muy bien
definidas y forman una estructura compleja alrededor del núcleo, dándole
un tamaño y forma algo indefinidas. Los resultados de su experimento le permitieron calcular que el radio atómico era diez mil veces mayor que el núcleo mismo, y en consecuencia, que el interior de un átomo está prácticamente vacío.
modelo en el cual el átomo
poseía un núcleo o centro en el cual se concentra la masa y la carga
positiva, y que en la zona extra nuclear se encuentran los electrones de
carga negativa.
Antes de que Rutherford propusiera su modelo atómico, los físicos aceptaban que las cargas eléctricas en el átomo tenían una distribución más o menos uniforme. Rutherford trató de ver cómo era la dispersión de las partículas alfa
por parte de los átomos de una lámina de oro muy delgada. Los ángulos
resultantes de la desviación de las partículas supuestamente aportarían
información sobre cómo era la distribución de carga en los átomos. Era
de esperar que, si las cargas estaban distribuidas uniformemente según
el modelo atómico de Thomson,
la mayoría de las partículas atravesarían la delgada lámina sufriendo
solo ligerísimas deflexiones, siguiendo una trayectoria aproximadamente
recta. Aunque esto era cierto para la mayoría de las partículas alfa, un
número importante de estas sufrían deflexiones de cerca de 180º, es
decir, prácticamente salían rebotadas en dirección opuesta a la
incidente.
La importancia del modelo de Rutherford residió en proponer por
primera vez la existencia de un núcleo en el átomo (término que,
paradójicamente, no aparece en sus escritos). Lo que Rutherford
consideró esencial, para explicar los resultados experimentales, fue
"una concentración de carga" en el centro del átomo, ya que sin ella, no
podía explicarse que algunas partículas fueran rebotadas en dirección
casi opuesta a la incidente. Este fue un paso crucial en la comprensión
de la materia, ya que implicaba la existencia de un núcleo atómico donde se concentraba toda la carga positiva y más del 99,9% de la masa. Las estimaciones del núcleo revelaban que el átomo en su mayor parte estaba vacío.
Rutherford propuso que los electrones
orbitarían en ese espacio vacío alrededor de un minúsculo núcleo
atómico, situado en el centro del átomo. Además se abrían varios
problemas nuevos que llevarían al descubrimiento de nuevos hechos y
teorías al tratar de explicarlos:
- Por un lado se planteó el problema de cómo un conjunto de cargas positivas podían mantenerse unidas en un volumen tan pequeño, hecho que llevó posteriormente a la postulación y descubrimiento de la fuerza nuclear fuerte, que es una de las cuatro interacciones fundamentales.
- Por otro lado existía otra dificultad proveniente de la electrodinámica
clásica que predice que una partícula cargada y acelerada, como sería
el caso de los electrones orbitando alrededor del núcleo, produciría radiación electromagnética, perdiendo energía y finalmente cayendo sobre el núcleo. Las leyes de Newton, junto con las ecuaciones de Maxwell del electromagnetismo aplicadas al átomo de Rutherford llevan a que en un tiempo del orden de
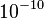 s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.2 Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.
s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.2 Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.
